Ministério da Saúde envia à Anvisa informações sobre a implementação dos autotestes de Covid-19
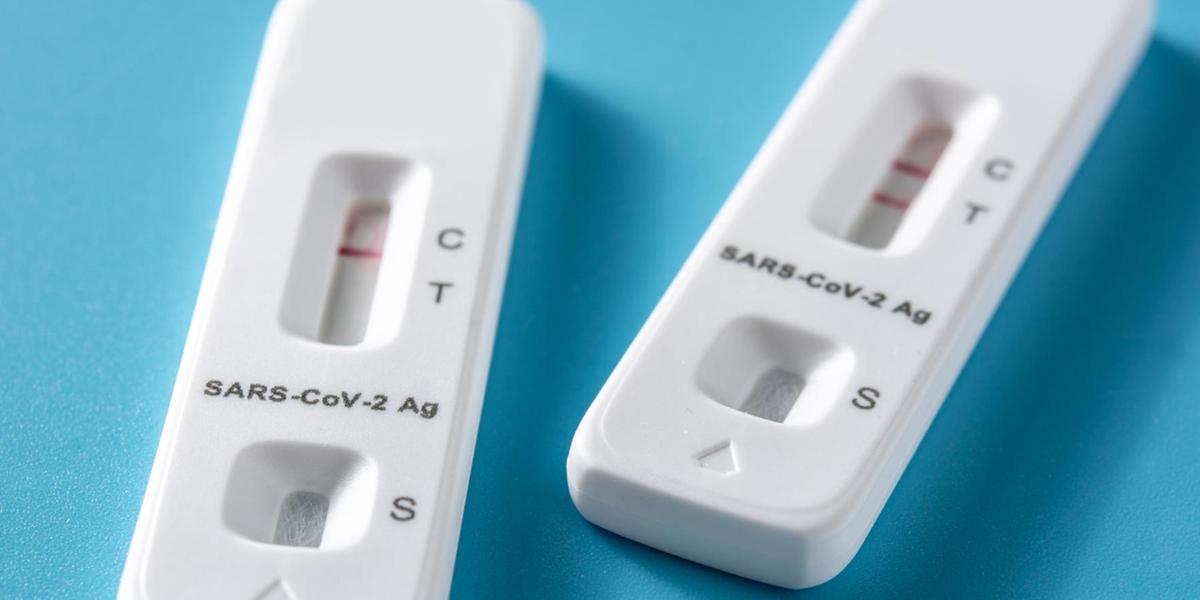
(Freepik / Divulgação)
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu do Ministério da Saúde (MS) informações sobre política pública para implementação dos autotestes de diagnóstico de Covid-19. As informações, de acordo com o ministério, foram encaminhadas à agência reguladora nessa terça-feira (25) à noite.
A agência confirmou o recebimento e disse que vai analisar as informações, mas não há prazo para resposta. Acrescentou, no entanto, que a deliberação sobre venda de autotestes deve sair no menor tempo possível.
A liberação de autotestes foi solicitada à Anvisa em 13 de janeiro. Na semana passada, a agência adiou a decisão e solicitou informações sobre como os testes seriam usados por pacientes leigos e como será feita a notificação dos resultados à Rede Nacional de Dados em Saúde do governo federal. Portaria do ministério determina que notificações de casos de coronavírus são compulsórias.
O ministério argumenta que a liberação dos testes vai ajudar no diagnóstico e tratamento da doença e que, se liberados, os autotestes devem integrar o Plano Nacional de Expansão da Testagem (PNE-Teste) para Covid-19.
"Se aprovada, medida será mais um eixo de apoio ao diagnóstico e monitoramento da situação epidemiológica do país. A orientação ao público sobre manuseio dos testes, conduta do usuário após o resultado e notificação do diagnóstico serão incluídos na nova edição do PNE-Teste", informou o MS.
Nesta quarta-feira (26), a Anvisa determinou o recolhimento de mais um autoteste de Covid-19 – o meuDNA PCR-LAMP Autocoleta de Saliva, da empresa Empreendimentos Pague Menos S/A. Nessa terça (25), a agência suspendeu a comercialização distribuição, fabricação, importação, propaganda e uso do Autoteste Covid-19 Isa Lab.
Em nota, a Anvisa informou que, "até o momento, não existe nenhum produto aprovado como autoteste, ou seja, para uso por usuários leigos".
Posicionamentos
Em nota enviada à Agência Brasil, a Isa Lab informou que o kit citado na matéria é um teste de detecção de Covid-19 que utiliza como base do diagnóstico a técnica PCR-LAMP (Amplificação Isotérmica Mediada por Loop) a partir de uma amostra de saliva, que é coletada pelo próprio paciente:
Segundo a empresa, o kit está registrado na Anvisa e está de acordo com a legislação e regulamentação vigentes. "A embalagem do produto foi desenvolvida quando a categoria de autotestes ainda não se fazia uma realidade no mundo. Por fim, até que haja uma reavaliação do entendimento da Anvisa quanto à suspensão presente, a Isa Lab retirou o produto de comercialização e reforça seu compromisso com a segurança e bem-estar dos clientes, que contam com um atendimento atestado pelo certificado ONA – uma metodologia de acreditação desenvolvida em 1999, a partir de métodos de certificação regionais da América Latina e de outros países, como Estados Unidos, Canadá, Espanha e Inglaterra, que tem por objetivo geral estimular o desenvolvimento de um processo permanente de avaliação e certificação da qualidade dos serviços de saúde", completa a nota.
A empresa meuDNA também enviou nota à Agência Brasil em que afirma que o kit de coleta de saliva vendido em farmácias é um produto registrado na Anvisa e está de acordo com a legislação e regulamentação vigentes. Segundo a empresa, o kit é utilizado para autocoleta domiciliares de amostras e subsequentemente são analisadas em laboratórios de análises clínicas:
A empresa disse ainda que espera que a Anvisa reavalie a "interpretação errônea e libere novamente os kits de autocoleta" o mais rápido possível.
Leia mais:
